Réponse : la majeure partie du sel que nous consommons vient de l'eau des mers et des océans. Les constituants de ce mélange homogène sont séparés par évaporation. Quels sont les facteurs favorisant l'évaporation ? Existe-t-il d'autres techniques de séparation des constituants d'un mélange homogène ?
I. L'évaporation
• L'évaporation est une méthode utilisée pour séparer les constituants d'un mélange homogène.
• L'eau salée est un mélange homogène formé de chlorure de sodium à l'état solide (le sel) et d'eau liquide, il faut effectuer une évaporation de l'eau pour récupérer le sel dissous.
• Protocole : un bécher rempli d'eau salée est placé sur une table au soleil.
• Observation : le niveau d'eau baisse très lentement et après quelques jours, les parois du bécher se couvrent d'une croûte de sel.
• Interprétation : l'évaporation de l'eau est un changement d'état. C'est la vaporisation de la surface libre de l'eau. Elle est généralement lente mais dépend de la température de l'eau, de l'humidité de l'air, de son agitation et de la dimension de la surface libre de l'eau en contact avec l'air.
• L'évaporation est couramment employée dans les marais salants pour extraire le sel. L'eau de mer est amenée dans de larges bassins de moins en moins profonds, où, sous l'effet de la chaleur du Soleil et du vent, elle s'évapore. Le sel fait son apparition et est alors collecté.
• Remarque : lorsque l'eau bout, elle ne s'évapore pas ; on dit qu'elle se vaporise. L'ébullition de l'eau est une vaporisation qui a lieu dans tout le liquide à une température bien définie et non pas en surface comme l'évaporation.
II. La distillation
• La distillation est un autre procédé permettant de séparer les constituants d'un mélange homogène. Le jus d'orange contient plusieurs constituants : sucre, arôme d'orange, eau, etc. Pour en extraire l'eau, nous pouvons procéder par distillation.
• La distillation permet de récupérer l'eau présente dans le mélange. Elle repose sur deux changements d'état inverses : la vaporisation et la liquéfaction. La vaporisation de l'eau permet de séparer l'eau, sous forme de vapeur, du reste du mélange. L'eau est ensuite récupérée sous la forme liquide par liquéfaction au contact d'une surface froide. Le liquide récupéré après distillation est appelé un distillat.
• Elle nécessite un montage un peu complexe.
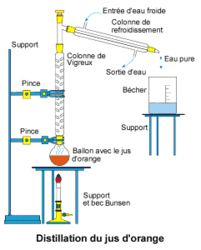 |
• Dans ce montage, on distingue deux parties : la colonne dans laquelle l'eau se vaporise et le refroidisseur qui servira à liquéfier l'eau à la sortie du dispositif. Le plus important est de bien contrôler la température de chauffage pour que seule l'eau se vaporise.
• Cette technique est également utilisée (dans un alambic, par exemple) pour séparer l'eau de l'alcool lors de la fabrication d'eau de vie. Mais, dans ce cas, c'est l'alcool qui est récupéré à la sortie du dispositif car sa température d'ébullition est plus basse que celle de l'eau.
III. La chromatographie
• Pour séparer les constituants d'un mélange homogène de colorants, nous procédons par chromatographie.
• Protocole : dans un bécher, nous versons l'éluant sur une hauteur de 1 cm. L'éluant est une solution d'eau salée et d'éthanol (alcool à brûler). Nous déposons une petite goutte d'une solution de colorant vert sur une bande de papier filtre, à 2 cm du bas. Le papier filtre est ensuite placé dans le bécher de sorte que le bas soit dans l'éluant sans que la tache de colorant ne soit en contact avec le liquide.
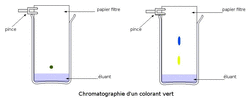 |
• Observation : l'éluant absorbé par le papier filtre monte et entraîne avec lui le colorant. Rapidement, les deux colorants qui composent la couleur verte (le jaune et le bleu) vont se séparer car le bleu monte plus vite que le jaune. Le colorant vert est donc un mélange de deux colorants, l'un bleu, l'autre jaune.
• Cette technique peut être utilisée également avec des encres et des peintures. La simplicité de sa mise en œuvre en fait une méthode d'analyse très utilisée en laboratoire de chimie. Elle est par exemple utilisée dans les laboratoires d'analyses médicales pour évaluer la quantité de vitamines dans le sang ; dans le domaine sportif pour savoir si un athlète s'est dopé ; mais également par la police scientifique pour analyser des substances prélevées sur une scène de crime.
Exercice n°1
Par quel procédé récupère-t-on le sel de l'eau de mer ?
Cochez la bonne réponse.
| ||
| ||
| ||
| ||
|
Ce procédé utilise l'action de la chaleur du Soleil.
L'évaporation est une méthode utilisée pour séparer les constituants d'un mélange homogène. L'eau salée est un mélange homogène formé de chlorure de sodium à l'état solide (le sel) et d'eau liquide, il faut effectuer une évaporation de l'eau pour récupérer le sel dissous. L'évaporation est la vaporisation de la surface libre de l'eau. Elle est généralement lente mais dépend de la température de l'eau, de l'humidité de l'air, de son agitation et de la dimension de la surface libre de l'eau en contact avec l'air.
Exercice n°2
La distillation est une technique de séparation des constituants d'un mélange.
Cochez la bonne réponse.
| ||
| ||
|
Cette technique est également utilisée dans un alambic, pour séparer l'eau de l'alcool.
La distillation est un autre procédé permettant de séparer les constituants d'un mélange homogène. Elle nécessite un montage un peu complexe : la colonne dans laquelle la substance à séparer se vaporise et le refroidisseur qui servira à liquéfier cette substance à la sortie du dispositif. Cette technique est également utilisée (dans un alambic, par exemple) pour séparer l'eau de l'alcool lors de la fabrication d'eau de vie. Mais, dans ce cas, c'est l'alcool qui est récupéré à la sortie du dispositif car sa température d'ébullition est plus basse que celle de l'eau.
Exercice n°3
Quelle est la proposition exacte ?
1. Les phénomènes physiques mis en jeu au cours d'une distillation sont :
Cochez la bonne réponse.
| ||
| ||
| ||
|
2. Le liquide obtenu après distillation est :
Cochez la bonne réponse.
| ||
| ||
|
La distillation repose sur deux changements d'état inverses.
La distillation repose sur deux changements d'état inverses : la vaporisation et la liquéfaction. Dans le cas de la distillation du jus d'orange, la vaporisation de l'eau permet de séparer l'eau, sous forme de vapeur, du reste du mélange. L'eau est ensuite récupérée sous la forme liquide par liquéfaction au contact d'une surface froide. Le liquide récupéré après distillation est appelé un distillat.
Exercice n°4
Complète la phrase suivante.
Écrivez les réponses dans les zones colorées.
Au cours d'une , les constituants d'un mélange sont séparés par un qui les entraînent à des vitesses différentes.
Au cours d'une chromatographie, les constituants d'un mélange sont séparés par un éluant qui les entraînent à des vitesses différentes. La simplicité de sa mise en œuvre en fait une méthode d'analyse très utilisée en laboratoire de chimie.
Elle est par exemple utilisée dans les laboratoires d'analyses médicales pour évaluer la quantité de vitamines dans le sang ; dans le domaine sportif pour savoir si un athlète s'est dopé ; mais également par la police scientifique pour analyser des substances prélevées sur une scène de crime.
Elle est par exemple utilisée dans les laboratoires d'analyses médicales pour évaluer la quantité de vitamines dans le sang ; dans le domaine sportif pour savoir si un athlète s'est dopé ; mais également par la police scientifique pour analyser des substances prélevées sur une scène de crime.

